继 FDA 批准后,Fresenius Kabi 的 tocilizumab-aazg (Tyenne) 成为第一个具有静脉 (IV) 和皮下制剂的托珠单抗 (Acterma) 生物仿制药。 Tocilizumab-aazg是一种称为白细胞介素 6 (IL-6) 受体拮抗剂的处方药。
继 FDA 批准后,Fresenius Kabi 的 tocilizumab-aazg (Tyenne) 成为第一个具有静脉 (IV) 和皮下制剂的托珠单抗 (Acterma) 生物仿制药。

Tocilizumab-aazg是一种称为白细胞介素 6 (IL-6) 受体拮抗剂的处方药。可阻断 IL-6 的作用,IL-6 是一种导致各种炎症性疾病的细胞因子。它由 Fresenius Kabi 采用先进的分析和制造技术开发,用于治疗多种自身免疫性疾病,包括类风湿性关节炎、巨细胞动脉炎、多关节幼年特发性关节炎和全身性幼年特发性关节炎。接受该产品的患者曾发生过导致住院或死亡的严重感染,包括结核病 (TB)、细菌、侵袭性真菌、病毒和其他机会性感染。
生物仿制药是一种生物制品,其批准的依据是证明其与已批准的生物制品高度相似,且在安全性和有效性方面与参比产品没有临床意义上的差异。Tyenne的批准得到了一项3期研究(ClinicalTrials.gov标识符:NCT04512001)数据的支持,该研究比较了tocilizumab-aazg与欧盟批准的tocilizumab在中度至重度活动性类风湿性关节炎患者中的疗效。
研究结果显示,基于第24周(主要终点)疾病活动评分-28关节计数-红细胞沉降率较基线的临床相关下降,两种产品具有同等疗效。在安全性和免疫原性方面也显示了相似性。
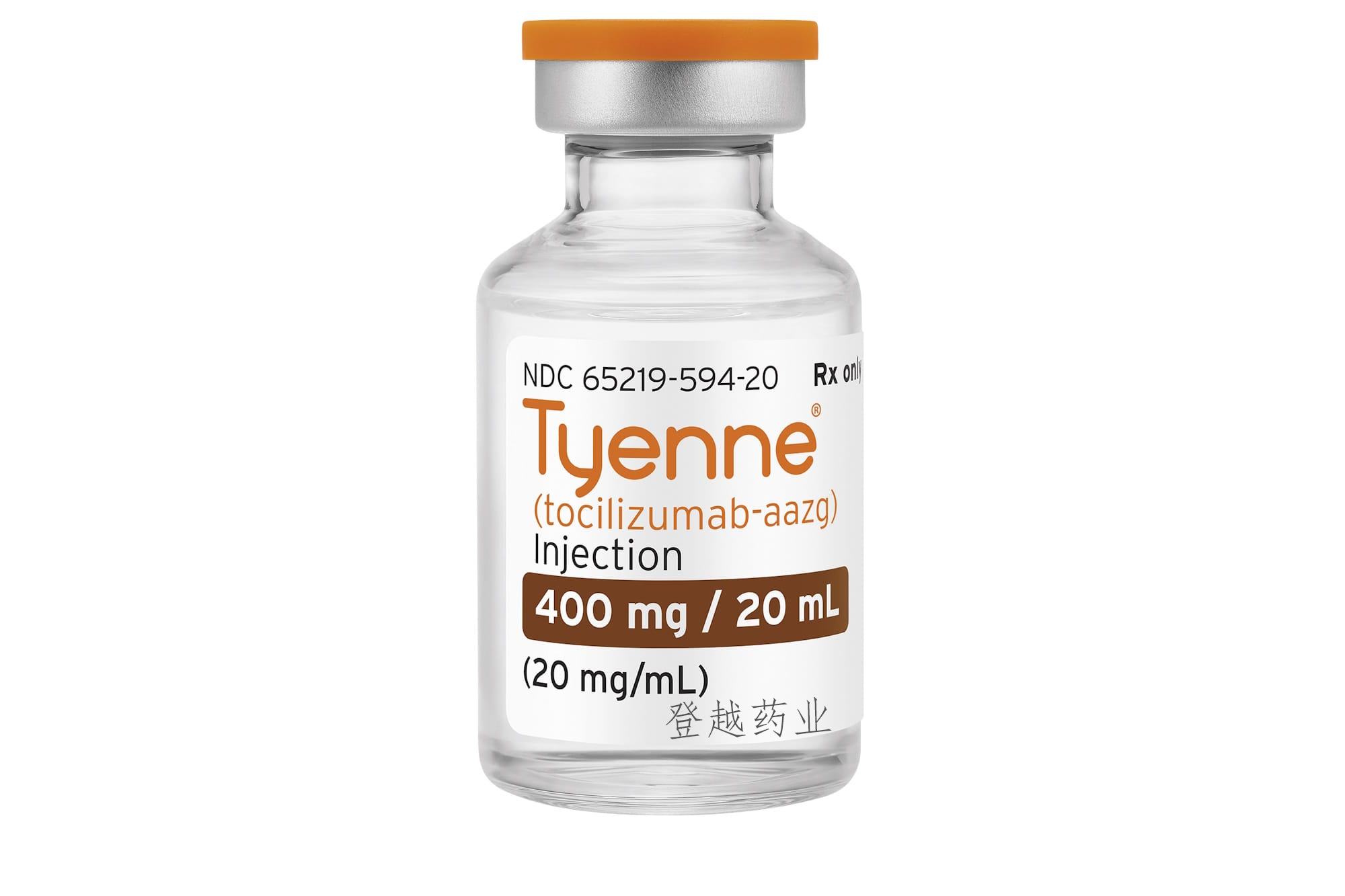
Tyenne以20mg/mL单剂量小瓶(80mg/4mL、200mg/10mL或400mg/20mL)形式提供,用于在静脉输注前进一步稀释。它还可作为即用型单剂量预装注射器 (162mg/0.9mL) 和用于皮下注射的单剂量预装自动注射器 (162mg/0.9mL) 提供。
注:本文旨在介绍药品健康研究分享,不作任何用药依据,具体用药指引,请咨询主治医师。
(责任编辑:登越药房)




